Применение микроэлементов кобальта и никеля в промышленной гидропонике
Российские специалисты не готовы к дальнейшей интенсификации производства огурца и томата – росту урожайности за счёт повышения мощности светильников и/или повышенных уровней углекислого газа. Эти факторы продуктивности приводят в первую очередь к стремительному росту (увеличению вегетативной массы) надземной части растения, при уменьшающемся соотношении корни/побеги (ведь объём субстрата остаётся тем же). Светокультура способствует ускоренному нарастанию новых и смене старых листьев, т. к. все физиологические процессы в растении ускоряются примерно в 2 раза. Существенно изменяется отношение листовой поверхности к общей массе растения. Соответственно должны значительно модифицироваться требования к минеральному питанию культуры, и поэтому следует критически посмотреть на классические голландские рекомендации конца прошлого века.
1. «Необходимые» и «полезные» микроэлементы для растений
Для роста и развития высшим растениям необходимо порядка 20 элементов питания. Два из них – углерод (в виде углекислого газа) и кислород – растения получают из воздуха и воды, остальные элементы поступают из почвы (субстрата). Традиционно элементы минерального почвенного питания делятся на две группы, в соответствии с потребностью в них растений:
– макроэлементы, которые требуются в больших количествах, их часто подразделяют на основные (N, P, K) и второстепенные (Ca, Mg, S) элементы питания;
– микроэлементы, которые необходимы в очень малых количествах (Fe, Mn, B, Zn, Cu, Mo, Cl, Na, Ni, Si, Co, Se).
Замечу, что к второстепенным элементам («мезоэлементам») нередко относят железо (Fe) и кремний (Si), т. к. они потребляются отдельными видами растений и/или при определённых условиях выращивания в значимых количествах. Кроме того, иногда описывают группу ультрамикроэлементов (V, Ti и другие). Это те элементы, содержание которых в растениях ничтожно мало, а физиологическая роль и влияние практически не изучены.
В группе мезо- и микроэлементов различают жизненно необходимые и полезные минеральные элементы. Жизненно необходимые минеральные элементы должны соответствовать трём критериям: (1) растения не способны завершить жизненный цикл при отсутствии данного элемента; (2) невозможно выполнение функций данного элемента другим элементом; (3) данный элемент непосредственно участвует в метаболизме растения.
К полезным минеральным элементам относятся питательные элементы, обладающие способностью стимулировать рост и развитие растений, но не в полной мере соответствующие требованиям, приведённым выше. К этой группе относятся и те элементы, которые необходимы либо в определённых условиях, либо для некоторых видов растений. Отсутствие полезных элементов питания может привести к тому, что потенциал сорта не будет полностью реализован в промышленных условиях выращивания. В литературе элементы питания делят на группы по-разному, это происходит потому, что для разных видов растений не одни и те же элементы являются жизненно необходимыми. В настоящее время к жизненно необходимым мезо- и микроэлементам относятся: Ca, Mg, S, Fe, Mn, B, Zn, Cu, Mo, Cl, Ni. К просто полезным причисляют мезо- и микроэлементы Na, Si, Co, Se, нередко I.
Вообще, чрезвычайно сложно измерить следовое количество химических элементов и доказать их роль в том или ином физиологическом процессе. Поэтому отдельные микроэлементы, не обнаруживаемые лабораторными методами в питательных средах, могут содержаться в них в виде примесей. Таких примесей оказывается достаточно для предотвращения проявления у растительного организма симптомов дефицита элемента.
2. Микроэлемент никель (Ni)
У большинства растений концентрация никеля в вегетативных органах колеблется от 1 до 10 мкг/кг сухой массы. Закономерности в распределении по органам объясняются повышенной мобильностью никеля во флоэме и ксилеме растений. Возможно, в растения ионы никеля поступают через активированные кальциевые каналы, так как специфических транспортёров никеля пока не найдено. Относительно недавно никель переведён из числа полезных в список необходимых микроэлементов.
В высших растениях наиболее хорошо изучен никельсодержащий фермент уреаза. Уреазы в них локализованы в вегетативных тканях и семенах, и участвуют в трансформации амидной формы азота. Никель, содержащийся в уреазе, не может быть замещён кобальтом без потери этим ферментом активности в растениях (Бобовые и Тыквенные). Очевидно, что потребность растений в никеле зависит от источника азотного питания, и, как следствие, без доставочного количества никеля использовать в гидропонике такое удобрение как мочевина бесполезно и даже вредно. Так, в экспериментальных условиях недостаток никеля вызывал нарушения метаболизма азота: подавлялась прорастание семян, отмечались избыточное накопление мочевины и некроз растительных тканей.
В высокой концентрации никель сильно токсичен для растений, впрочем, как и все другие микроэлементы. Негативное действие на растения связано с индицированием ими окислительного стресса, блокированием функциональных групп молекул, вытеснением других микроэлементов, входящих в состав ферментов. Неспецифический механизм токсического действия состоит в ингибировании поглощения корнями ионов других питательных элементов. При избытке никеля снижалось поглощение растениями железа и магния, что сопровождалось появлением признаков хлороза вторичного происхождения.
К распространённым никелевым удобрениям относится сульфат никеля NiSO₄⋅7H₂O. Но, как и в ситуации с железом, никель в почвах и растворах часто становится трудно доступным для растений.
3. Микроэлемент кобальт (Co)
Кобальт найден во всех низших и высших растениях, где он содержится в количестве от 0.05 до 11.5 мг/кг сухого вещества. В растениях примерно 50% кобальта находится в ионной форме, 20% – в форме кобамидных соединений и в составе витамина В₁₂. До 30% соединений составляют неидентифицированные стабильные органические соединения.
Витамином B₁₂ называют группу биологически активных веществ – кобаламинов, содержащим в структуре атом кобальта (III), и являющиеся разновидностью хелатных соединений. Данный витамин синтезируется микроорганизмами и поступает в растения из почвы, у азотфиксирующих растений образуется в клубеньках. Большинству растений сам по себе витамин B₁₂ для нормальной жизнедеятельности не требуется, и они его вообще не синтезируют. Поэтому фрукты, овощи и зерновые культуры практически не содержат витамина B₁₂. Небольшое количество этого витамина может также накапливаться в растениях в результате взаимодействия с почвенными бактериями.
Долгое время считали, что кобальт необходим только животным и микроорганизмам, и что для растений он не является необходимым элементом. Вместе с тем известные факты, свидетельствующие о роли кобальта как активатора большого количества ферментов, и данные о значении его для регуляции роста, а также о многообразном влиянии его на обмен веществ, поставили под сомнение представления многих исследователей о ненужности этого элемента растениям. Наиболее чувствительны к дефициту кобальта бобовые культуры, сахарная свекла, пшеница, рис и виноград. Отмечен как значительный положительный эффект кобальта на рост томатов, так и отсутствие каких-либо внешних признаков кобальтовой недостаточности.
Традиционно функции кобальта рассматривают в связи с его участием в фиксации атмосферного азота в клубеньках бобовых и не бобовых растений. Участие кобальта в метаболизме высших растений, не способных к азотофиксации, может быть прямым или косвенным. Одной из ролей кобальта является его физиологическое воздействие на окислительно-восстановительные процессы, которые протекают в живой клетке растения. Он принимает участие в переносе фосфатных групп, в процессах карбоксилирования, гидролиза пептидных связей и фосфорных эфиров. Кобальт активизирует ряд ферментов (киназа и энолаза пировиноградной кислоты), снижает активность пероксидазы, благодаря чему замедляется распад индолилуксусной кислоты. Кобальт принимает участие в биосинтезе белка, и связан с нуклеиновым обменом. Кобальт важнейшим образом влияет на процессы дыхания и энергетического обмена у растений. Известны по крайне мере три важных фермента, зависимых от кобальта. Установленная роль кобальта в энергетическом и нуклеиновом обмене и в белковом синтезе, является прямым доказательством полезности и необходимости для растений. Помимо этого, кобальт увеличивает количество аскорбиновой кислоты в тканях растения.
Кобальт влияет на формирование и функционирование фотосинтетического аппарата растений. Доказано влияние кобальта на формирование и функционирование фотосинтетического аппарата растений посредством концентрации пигментов и хлоропластов в листьях, что непосредственно связано с ростом объёма пластидного аппарата и органелл. Кобальт также накапливается в генеративных органах, и ускоряет прорастание пыльцы. Последнее наводит на мысль о полезности кобальта для процессов оплодотворения.
Объяснением причин ростового эффекта кобальта могут служить данные о связи этого микроэлемента с ауксиновым обменом. Ионы кобальта влияют на гормональный обмен растения, ингибируя образование этилена и инактивируя ауксиноксидазу. Ауксиноксидаза – фермент, регулирующий уровень ауксинов в тканях. Если активировать этот фермент, они будут разрушаться, и рост органов растения замедлится. Если подавить активность этого фермента, то уровень ауксинов, наоборот, возрастёт и рост органов усилится. То есть, воздействуя на активность системы ауксиноксидаза-ауксин, они регулируют уровень ауксинов. В частности, такой способ устранения пустотелости плодов с помощью увеличения концентрации ауксинов в завязях томата рассматривается в теме «Причины образования пустотелых плодов у томата» (https://greentalk.ru/topic/18833/).
Стимуляция роста кобальтом объясняется участием этого микроэлемента также и в пролонгированном ингибировании продуцирования этилена. Возможно, торможение синтеза эндогенного этилена ионами кобальта, приводит к повышению компетентности тканей и к экзогенному этилену.
Недостаток кобальта у отдельных видов растений внешне проявляется аналогично признакам дефицита азота: короткий цикл развития, замедление роста, хлороз листьев. В избыточных концентрациях кобальт тормозит поглощение и транспорт из корней в побеги железа и марганца, вызывая у растений симптомы хлороза вторичного происхождения.
Объяснения улучшенного роста не бобовых растений при использовании кобальтосодержащих удобрений различаются, но их можно обобщить следующим образом:
(1) повышенная устойчивость к абиотическим стрессам,
(2) активация антиоксидантных ферментов,
(3) способность заменять другие переходные металлы в большом количестве ферментов, и
(4) гормезис (лёгкая стимуляция какой-либо системы организма).
Сообщалось, что применение кобальта облегчает недостаток воды, стресс от тяжелых металлов, а также увеличивало накопление свободного пролина, что противодействовало солевому стрессу. В целом абиотические стрессы вызывают у растений дисбаланс между образованием и накоплением активных форм кислорода (АФК). Кобальт, применяемый в соответствующих концентрациях, может активировать антиоксидантные ферменты, тем самым уменьшая повреждение, вызванное АФК.
Из-за ограниченных исследований кобальта на сегодняшний день эти объяснения могут быть неточными и неполными. Обоснованное предположение авторов состоит в том, что применение соответствующего количества кобальта может стимулировать ризосферные (симбиотические, эндофитные, либо ассоциированные) бактерии фиксировать атмосферный азот, тем самым повышать содержание азота в почве и усиливать рост как бобовых, так и растений из других семейств. Если такое положение верно, то и в тепличных субстратах достаточное наличие ионов кобальта должно способствовать активному развитию полезного микробного биоценоза? Возможно, на этот вопрос смогут ответить А.К. Ахатов (ШЕТЕЛИГ РУС) или Н.С. Марквичев (БИОМ-ПРО).
В то же время, Co-содержащие ферменты могут быть активированы для надлежащей биохимической и физиологической активности. Например, карбонатдегидратаза может усиливать фотосинтез, а Co-пероксидаза может активировать ферментативную антиоксидантную систему. В результате растения будут поглощать больше питательных веществ, и также улучшать свой рост и общую стрессоустойчивость.
Самая удивительная способность кобальта состоит в возможности заменять некоторые элементы питания, если они имеют ограниченную доступность. Такая характеристика тесно связана с физико-химическими свойствами кобальта. Ионный радиус Co²⁺ составляет 0,76 Å, что сопоставимо с 0,74 Å Zn²⁺, 0,69 Å Cu²⁺ и 0,76 Å Fe²⁺. Правда, эти ферменты в основном встречаются у животных, бактерий и дрожжей, и лишь некоторые – у растений.
Кроме того, на основе доступных структур из Protein Data Bank обнаружено, что Co²⁺ обычно связывается катионными ловушками. Ловушки образованы относительно отрицательно заряженными участками клубка белковой спирали, в которых расположены остатки аминокислот гистидина, аспарагина и глутамата. Эти позиции обычно заняты ионами других металлов, таких как Cu²⁺, Mg²⁺, Mn²⁺ и Zn²⁺, которые играют значительную роль в качестве катализаторов. В результате ион кобальта вполне мог заменять эти ионы в активных центрах ферментов. Таким образом, кобальт способен замещать медь, железо, никель и цинк в активных центрах ферментов. Кстати, по этим причинам ферменты или белки, специфичные именно для кобальта, окончательно не идентифицированы.
Замена тетраэдрического иона цинка более высоко координированным ионом кобальта неожиданно часто приводит к образованию активного соединения с каталитическими свойствами исходного фермента. В подавляющем большинстве случаев, никакой другой ион переходного металла, кроме Co²⁺, не обеспечивает лучшей замены Zn²⁺.
К кобальтовым удобрениям относятся сульфат кобальта CoSO₄⋅7H₂O, хлорид кобальта CoCl₂⋅6H₂O и нитрат кобальта Co(NO₃)₂⋅6H₂O. В настоящее время многие изготовители минеральных удобрений выпускают хелат кобальта (13% Co-EDTA).
4. Вопросы с кобальтом и никелем
Никель и кобальт тесно связаны геохимически. Соединения кобальта получают в основном при переработке никелевых руд, в которых массовая доля этого элемента составляет 0,15-0,2%. В качестве примесей кобальт содержится во многих удобрениях: фосфоритной муке, суперфосфате, томасшлаке, пиритных огарках. Без сомнения, как примесь в них присутствует и никель в достаточных количествах. Также микроэлементами специально обогащают аммофос, карбоаммофоску, нитродиаммофос, нитроаммофоску, нитрофоску и другие. Содержание микроэлементов в этих удобрениях колеблется в зависимости от технологии изготовления: марганец 1-3%, цинк 0,3-0,8%, медь 0,6-0,9%, бор 0,2-0,5%, кобальт 0,1%.
По крайней мере, для выращиваемых в почве культур микроэлементы никель и кобальт естественным образом доступны из почвы или из примесей в минеральных и органических удобрениях. Однако с Ni и Co недостаточно или вообще не проводятся какие-либо исследования для тепличного производства, точнее в промышленной гидропонике. Риск того, что важные микроэлементы станут недоступными для тепличных культур, возрастает, если используемые субстраты будут свободны от минеральных следов, а применяемые удобрения и поливная вода становятся все более свободными от каких-либо фоновых концентраций. Но моему мнению, с никелем особой проблемы пока не отмечается, поскольку он явно содержатся как примесь в других минеральных удобрениях, поливной воде и, возможно, в базальтовых субстратах, а вот с кобальтом ситуация не совсем простая.
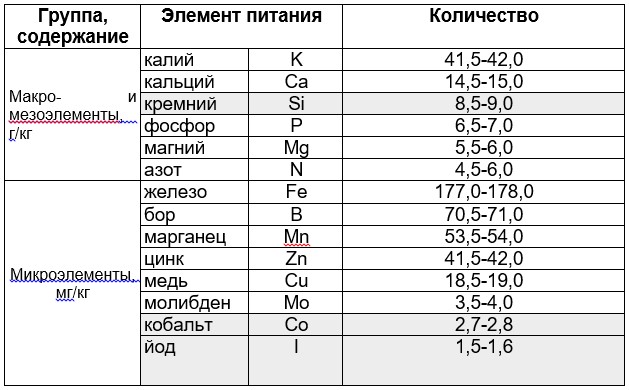
Базы удобрений в агрохимических программах NSC (L. Incrocci), Агроном (ФИТО) и Агрохимик (Королев-Агро) вообще не содержат соединения кобальта (Co). То есть, согласно классическим голландским рецептам в тепличном производстве данный микроэлемент не обязателен. Против этого положения есть серьёзные возражения. Так, содержание того или иного элемента в растениях считается систематическим признаком, который формируется эволюционно и передаётся по наследству. Посмотрим данные по тепличному огурцу (табл. 1), и видим очень значительное поглощение и накопление этим растением таких, казалось бы, «ненужных» элементов как кремний, кобальт и йод.
Таблица 1
Содержание элементов питания в листьях тепличного огурца, на сухую массу